2024年10月31日,深圳大學醫學部助理教授李國鋒與中山大學教授洪亮、教授李民等合作,在美國化學會藥物化學權威期刊Journal of Medicinal Chemistry上發表題為“Design, synthesis and activity evaluation of BRD4 PROTAC based on alkenyl oxindole-DCAF11 pair”的研究論文。一種基于雙熒光報告細胞系的高內涵篩選策略,成功實現了蛋白靶向嵌合體(PROTAC)的快速篩選。此外,研究進一步證實了烯基氧化吲哚與E3泛素連接酶DCAF11在PROTAC設計中的互配關系。這一發現對新型E3泛素連接酶配體的發現與應用具有重要的推動意義。深圳大學醫學部博士后趙漫,碩士研究生馬文靜、梁錦怡為該研究的共同第一作者。

靶向蛋白降解(TPD)是一種新興的治療策略,通過誘導不可成藥蛋白的降解從而達到治療目的,其中最具代表性的PROTAC分子備受關注并已進入臨床研究階段,表明了PROTAC的應用潛力。然而,逐漸顯現的耐藥性及PROTAC活性鑒定的低效性限制了PROTAC的快速發展。因此,開發有效的高通量篩選策略對PROTAC的發展具有重要意義。
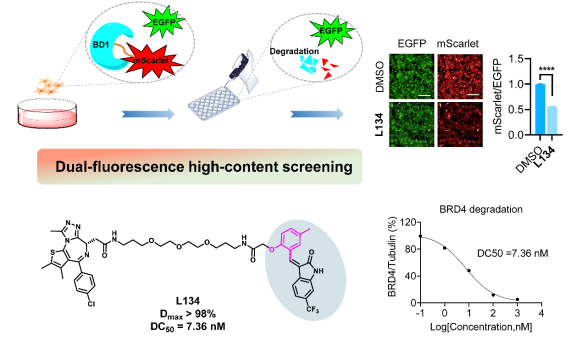
該研究團隊在先前研究的基礎上(PLOS Biol.2024,22, e3002550),新設計合成了一系列基于烯基氧化吲哚結構的BRD4-PROTAC先導化合物。采用mScarlet/ EGFP的雙熒光報告細胞系,結合細胞高內涵成像技術,實現了細胞中靶蛋白降解效率的高通量高效率評估。通過這種高通量篩選策略,該團隊篩選獲得了一種強效的BRD4-PROTAC先導化合物L134(Dmax> 98%, DC50= 7.36 nM)。L134不僅能顯著抑制多種乳腺癌細胞的增殖,還可抑制乳腺癌細胞遷移并誘導細胞凋亡,表明了L134的抗乳腺癌潛力。
這一研究成果不僅證實了基于高內涵的高通量靶向蛋白質降解篩選的有效性,也進一步證實了烯基氧化吲哚與DCAF11在蛋白降解中的應用潛力,為靶向蛋白質降解藥物的研發和應用提供了有價值的借鑒。
該研究得到了國家自然科學基金委等項目的支持。
原文鏈接:https://doi.org/10.1021/acs.jmedchem.4c01767





